Ácido nucleico de Mycobacterium tuberculosis y resistencia a la rifampicina
Nombre del producto
HWTS-RT074B - Kit de detección de ácido nucleico de Mycobacterium tuberculosis y resistencia a la rifampicina (curva de fusión)
Certificado
CE
Epidemiología
Mycobacterium tuberculosis, abreviado como bacilo tuberculoso o TB, es la bacteria patógena que causa la tuberculosis. Actualmente, los fármacos antituberculosos de primera línea más utilizados incluyen isoniazida, rifampicina y hexambutol, entre otros. Los fármacos de segunda línea incluyen fluoroquinolonas, amikacina y kanamicina, entre otros. Los fármacos de reciente desarrollo son linezolid, bedaquilina y delamani, entre otros. Sin embargo, debido al uso incorrecto de los fármacos antituberculosos y a las características de la estructura de la pared celular de Mycobacterium tuberculosis, esta bacteria desarrolla resistencia a los fármacos antituberculosos, lo que supone un grave desafío para la prevención y el tratamiento de la tuberculosis.
La rifampicina se ha utilizado ampliamente en el tratamiento de pacientes con tuberculosis pulmonar desde finales de la década de 1970, con resultados significativos. Ha sido la primera opción para acortar la quimioterapia en estos pacientes. La resistencia a la rifampicina se debe principalmente a la mutación del gen rpoB. Si bien constantemente se desarrollan nuevos fármacos antituberculosos y la eficacia clínica en pacientes con tuberculosis pulmonar ha mejorado, aún existe una relativa escasez de medicamentos y el uso irracional de fármacos en la práctica clínica es relativamente frecuente. Evidentemente, la Mycobacterium tuberculosis en pacientes con tuberculosis pulmonar no se elimina por completo de manera oportuna, lo que eventualmente conduce a diferentes grados de resistencia a los fármacos en el organismo del paciente, prolonga el curso de la enfermedad y aumenta el riesgo de muerte.
Canal
| Canal | Canales y fluoróforos | Tampón de reacción A | Tampón de reacción B | Tampón de reacción C |
| Canal FAM | Reportero: FAM, Quencher: Ninguno | rpoB 507-514 | rpoB 513-520 | 38KD e IS6110 |
| Canal CY5 | Reportero: CY5, Supresor: Ninguno | rpoB 520-527 | rpoB 527-533 | / |
| Canal HEX (VIC) | Reportero: HEX (VIC), Supresor: Ninguno | Control interno | Control interno | Control interno |
Parámetros técnicos
| Almacenamiento | ≤-18℃ En la oscuridad |
| Duración | 12 meses |
| Tipo de muestra | Esputo |
| CV | ≤5,0% |
| LoD | Mycobacterium tuberculosis 50 bacterias/mL tipo salvaje resistente a la rifampicina: 2x103bacterias/mL mutante homocigoto: 2x103bacterias/mL |
| Especificidad | Detecta la micobacteria tuberculosis de tipo salvaje y los sitios de mutación de otros genes de resistencia a fármacos como katG 315G>C\A, InhA-15C> T, los resultados de la prueba no muestran resistencia a la rifampicina, lo que significa que no hay reactividad cruzada. |
| Instrumentos aplicables: | Sistemas de PCR en tiempo real SLAN-96P Sistema de PCR en tiempo real BioRad CFX96 Sistema de PCR en tiempo real LightCycler480® |
Flujo de trabajo
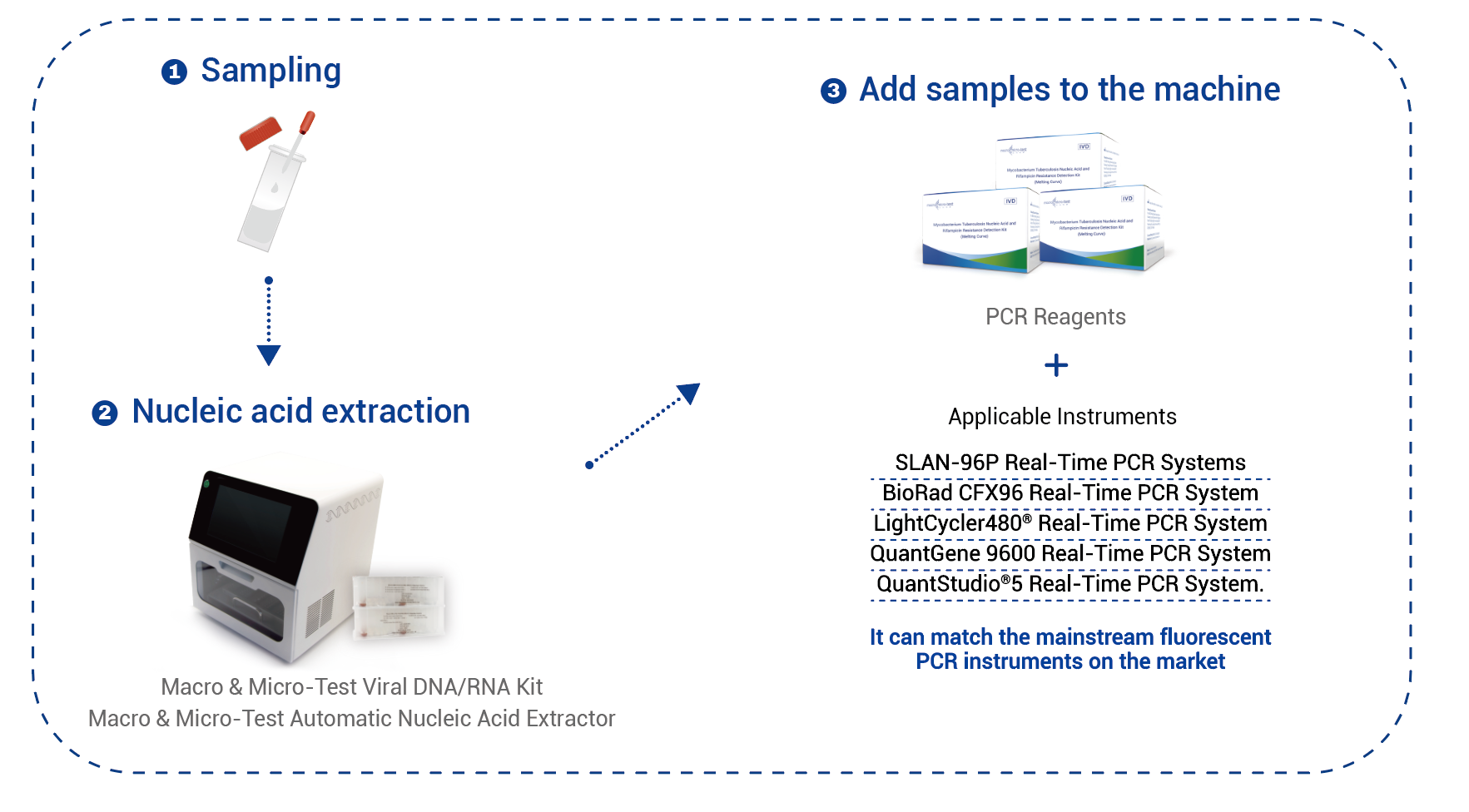
Si se utiliza el kit general de ADN/ARN Macro & Micro-Test (HWTS-3019-50, HWTS-3019-32, HWTS-3019-48, HWTS-3019-96) (que se puede utilizar con el extractor automático de ácidos nucleicos Macro & Micro-Test (HWTS-3006C, HWTS-3006B)) o la columna de ADN/ARN viral Macro & Micro-Test (HWTS-3022-50) de Jiangsu Macro & Micro-Test Med-Tech Co., Ltd. para la extracción, agregue 200 μL del control positivo, el control negativo y la muestra de esputo procesada que se va a analizar en secuencia, y agregue 10 μL del control interno por separado al control positivo, al control negativo y a la muestra de esputo procesada que se va a analizar, y los pasos subsiguientes deben llevarse a cabo estrictamente de acuerdo con las instrucciones de extracción. El volumen de muestra extraído es de 200 μL, y el volumen de elución recomendado es de 100 μL.