I. Descripción general de laESMODirectriz de 2025
En agosto de 2025, la ESMO publicó oficialmente la Guía de Práctica Clínica de la ESMO para el diagnóstico, tratamiento y seguimiento del cáncer de pulmón de células no pequeñas en estadio temprano y localmente avanzado, en la prestigiosa revista oncológica Annals of Oncology. Esta es la primera actualización exhaustiva desde la versión de 2017 y constituye una referencia de gran autoridad para los oncólogos de todo el mundo.

El cáncer de pulmón presenta la mayor incidencia y mortalidad de todas las neoplasias malignas a nivel mundial. Cada año, se registran más de 2,2 millones de casos nuevos y más de 1,8 millones de fallecimientos, lo que lo convierte en la principal causa de muerte por cáncer tanto en hombres como en mujeres. El cáncer de pulmón de células no pequeñas (CPCNP) representa aproximadamente el 80-85% de todos los casos de cáncer de pulmón. Ante esta grave situación, la publicación de la guía de 2025 impulsa la práctica clínica, siendo la actualización de las estrategias de análisis de biomarcadores particularmente crucial.
II. Interpretación de las principales actualizaciones de las directrices
2.1 Pruebas de biomarcadores: De “opcionales” a “esenciales”
La guía de 2025 introduce un ajuste estratégico trascendental con respecto a las pruebas de biomarcadores. La guía establece explícitamente que las pruebas de biomarcadores son esenciales para la toma de decisiones terapéuticas en pacientes con cáncer de pulmón no microcítico en estadio IB-III.
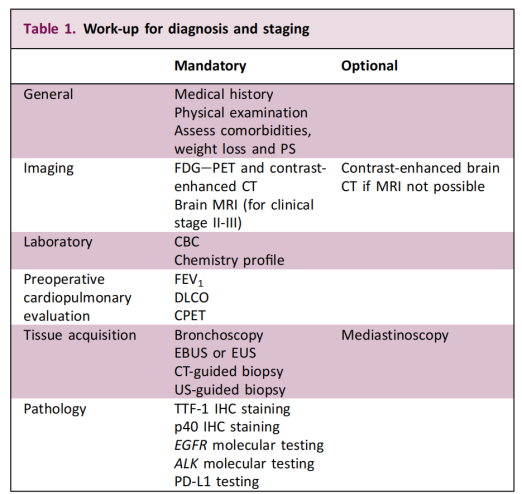
Esta recomendación amplía las pruebas moleculares, que antes se centraban en pacientes con enfermedad avanzada, a casos resecables en estadios tempranos. El objetivo principal es identificar mutaciones genéticas clave y proporcionar una base científica para un tratamiento de precisión personalizado. La guía también subraya que la viabilidad de la biopsia y el enfoque diagnóstico deben ser determinados por un equipo multidisciplinario en función de las características del paciente y del tumor.
En cuanto a la estrategia de pruebas específicas, la guía recomienda claramente que las pruebas genéticas se realicen antes de tomar la decisión quirúrgica y que, como mínimo, abarquen los genes EGFR y ALK. Este concepto de "pruebas previas" tiene una profunda relevancia clínica para la estratificación precisa y el tratamiento personalizado del cáncer de pulmón no microcítico en estadio temprano; la puntualidad y la precisión de los resultados de las pruebas determinan directamente la elección de la terapia adyuvante posterior.
2.2 Avances terapéuticos en el cáncer de pulmón de células no pequeñas en estadio temprano con oncogenes impulsores positivos
La guía de 2025 integra la evidencia de múltiples estudios clínicos importantes para establecer una vía de tratamiento de precisión clara para pacientes con cáncer de pulmón de células no pequeñas en estadio temprano con oncogenes impulsores positivos.
Pacientes con mutación positiva del EGFR:Basándose en el emblemático ensayo ADAURA, el tratamiento adyuvante posoperatorio con osimertinib durante tres años se ha convertido en el estándar global para pacientes con deleciones del exón 19 del EGFR o mutaciones L858R del exón 21. El ensayo ADAURA es un estudio internacional, multicéntrico, aleatorizado y controlado de fase III que evalúa la eficacia y la seguridad del osimertinib adyuvante en pacientes con cáncer de pulmón no microcítico (CPNM) con mutación del EGFR en estadios IB-IIIA completamente resecados. El estudio demostró que el osimertinib mejoró significativamente tanto la supervivencia libre de enfermedad como la supervivencia global en comparación con el placebo, estableciéndolo como el nuevo estándar de tratamiento para esta población. Sin embargo, los análisis exploratorios del ensayo ADAURA indicaron que aproximadamente el 36 % de las interrupciones tempranas del tratamiento se debieron a eventos adversos, y otro 31 % a decisiones del paciente. Este hallazgo subraya la necesidad de realizar pruebas basales precisas antes del tratamiento para garantizar que la terapia dirigida se administre a los pacientes que pueden obtener un beneficio sostenido.
Pacientes ALK-positivos:Basándose en el ensayo ALINA, el tratamiento adyuvante posoperatorio con alectinib durante dos años es ahora el estándar de atención. En el análisis primario del ensayo ALINA, un estudio aleatorizado abierto de fase III, alectinib demostró un marcado beneficio en la supervivencia libre de enfermedad en la población con estadio II-IIIA, con un cociente de riesgos de 0,24. Los datos actualizados del ensayo ALINA, presentados en el congreso ESMO 2025, mostraron que, tras ≥3 años de seguimiento, el beneficio de alectinib en la supervivencia libre de enfermedad se mantuvo "sostenido y clínicamente significativo", con un cociente de riesgos de 0,36 en la población con estadio II-IIIA. La tasa de supervivencia global a 4 años más reciente alcanzó el 98,4%, la tasa de supervivencia libre de enfermedad a 4 años fue del 75,5%, y la supervivencia libre de enfermedad del sistema nervioso central también mejoró, sin nuevas señales de seguridad. Estos datos sólidos consolidan aún más el tratamiento adyuvante con alectinib como estándar de atención tras la resección de un cáncer de pulmón no microcítico ALK-positivo y subrayan la importancia de realizar pruebas precisas para identificar a estos pacientes.
Elección del método de prueba:La guía ESMO 2025 enumera explícitamenteEnsayos de panel de RT-PCR multiplexJunto con la secuenciación de nueva generación (NGS) basada en ARN, la inmunohistoquímica (IHC) y la hibridación fluorescente in situ (FISH), se recomiendan estas técnicas para la detección de la fusión ALK. Esto indica que el requisito fundamental de la guía es realizar pruebas para orientar las decisiones clínicas, en lugar de imponer una plataforma de pruebas específica. Para los productos de RT-PCR centrados en la detección de EGFR y ALK, esta estrategia de pruebas flexible proporciona una sólida justificación, basada en las guías, para su uso en la práctica clínica.
III. Soluciones técnicas para ensayos de precisión
La guía de 2025 traslada las pruebas a la etapa de toma de decisiones prequirúrgicas, lo que eleva los estándares de precisión, sensibilidad y accesibilidad de los ensayos. Los dos productos de detección basados en RT-PCR que se describen a continuación se ajustan con precisión a los requisitos de la guía desde una perspectiva técnica.
3.1 Kit de detección de mutaciones del EGFR: plataforma tecnológica ARMS mejorada
Tecnología centralLa tecnología ARMS mejorada permite la amplificación específica de secuencias mutantes de baja abundancia frente a un fondo de tipo silvestre elevado.
Tres medidas de seguridad técnicas:
-ARMS mejorado → mejora el reconocimiento de mutaciones
-Enriquecimiento enzimático → digiere el fondo de tipo silvestre y enriquece las secuencias mutantes
-El bloqueo de temperatura suprime la amplificación no específica.
Actuación: Sensibilidad deFrecuencia del alelo mutante del 1%
Control de la contaminación: El control interno incorporado y la enzima UNG previenen la contaminación.
Tiempo de respuesta: Funcionamiento en tubo cerrado, aproximadamente120 minutos
Compatibilidad de muestras:Tejido/biopsia líquidamuestras → aborda el requisito de “pruebas previas”
Cobertura:45 mutacionesen los exones 18-21 del EGFR, coincidiendo exactamente con las regiones resaltadas en las directrices (deleciones del exón 19 y L858R del exón 21).
Uso clínicoGuía directamente la terapia con EGFR-TKI.
3.2 Kit de detección de fusión MMT EML4-ALK – Solución de detección de fusión basada en ARN

-Plataforma tecnológicaRT-PCR basada en ARN: ofrece ventajas inherentes sobre los métodos basados en ADN para la detección de fusiones.
-Ventaja basada en ARNDetecta directamente los transcritos de fusión expresados, evitando eficazmente los falsos negativos.
-Evidencia del estudioEn fusiones ALK de baja abundancia, la RT-PCR es significativamente más fiable que las pruebas basadas en ADN.
-Sensibilidad: Detecta fusiones hasta20 copias por reacción
-Cobertura de variantes: Cubiertas12 variantes comunes de fusión EML4-ALK(incluida la variante 1 ~33%; variantes 3a/3b juntas ~29%)
-Operación y control de la contaminación: Tubo cerrado, ~120 minutos; los controles de proceso integrados + la enzima UNG evitan resultados falsos.
-Compatibilidad de instrumentos: Compatible con varios instrumentos de PCR en tiempo real de uso común.
-Alineación con las directrices: Altamente coherente con la guía de la ESMO
IV. Coherencia entre los ensayos y las recomendaciones de las directrices
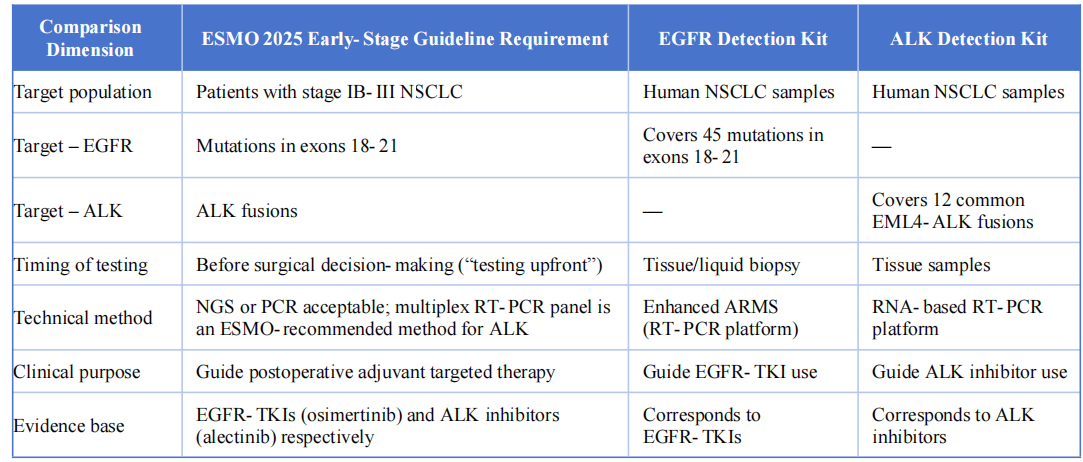
Los dos productos de detección son altamente consistentes con la guía ESMO 2025 para el cáncer de pulmón de células no pequeñas en estadio temprano y localmente avanzado en las siguientes dimensiones clave:
V. Conclusión
La guía ESMO 2025 para el cáncer de pulmón de células no pequeñas en estadio temprano inaugura una nueva era de diagnóstico y tratamiento de precisión, centrada en “Pruebas previas, focalización precisa y optimización del tratamiento.“El kit de detección de mutaciones EGFR y el kit de detección de fusión MMT EML4-ALK cumplen con los requisitos de las directrices en cuanto a objetivos, tiempos y precisión mediante distintas vías técnicas.
El kit EGFR utiliza tecnología ARMS mejorada para la detección de alta sensibilidad de mutaciones específicas en muestras limitadas, lo que permite realizar tanto biopsias de tejido como líquidas y posibilita la realización de pruebas de forma anticipada.
El kit ALK se basa en la RT-PCR basada en ARN, lo que ofrece ventajas sobre los métodos de ADN para la detección de fusiones, en consonancia con la recomendación de ESMO de utilizar paneles de RT-PCR multiplex para las pruebas de ALK.
En conjunto, estos dos productos conforman una solución de análisis de precisión que cumple con la guía ESMO 2025 y que respalda la terapia adyuvante personalizada para el cáncer de pulmón no microcítico en etapa temprana.
Referencias:
- Zer A, Ahn MJ, Barlesi F, et al. Cáncer de pulmón de células no pequeñas en estadio temprano y localmente avanzado: Guía de práctica clínica de la ESMO para el diagnóstico, tratamiento y seguimiento. Ann Oncol. 2025;36(11):1245-1262. doi:10.1016/j.annonc.2025.08.003
Fecha de publicación: 6 de mayo de 2026

