El 24 de marzo de 2026 se conmemora el 31.º Día Mundial de la Tuberculosis. La Organización Mundial de la Salud (OMS) ha anunciado el tema mundial de este año como“¡Sí! ¡Podemos acabar con la tuberculosis!”Haciendo hincapié en que un liderazgo gubernamental sólido, un compromiso político sostenido y una acción multisectorial coordinada son esenciales para acabar con la epidemia de tuberculosis (TB).

Progreso global y desafíos pendientes
Según el Informe Mundial sobre la Tuberculosis 2025, el control mundial de la tuberculosis alcanzó un hito significativo en 2024, con ambosLa incidencia y la mortalidad están disminuyendo.Por primera vez desde la pandemia de COVID-19.
Se estima que10,7 millones de personasdesarrollaron tuberculosis en 2024, incluyendo 54% hombres, 35% mujeres y 11% niños y adolescentes. Entre estos casos, aproximadamente619.000 (5,8%)estaban coinfectados con VIH y390.000 (3,6%)eran tuberculosis multirresistente o resistente a la rifampicina (TB-MDR/RR).
La tuberculosis causó aproximadamente1,23 millones de muertesEn 2024, la tuberculosis siguió siendo la principal causa infecciosa de muerte a nivel mundial, superando a la COVID-19. Tras tres años de aumentos entre 2021 y 2023, la incidencia mundial de tuberculosis disminuyó en casi un 2 % en 2024, lo que refleja una recuperación gradual de los servicios de tuberculosis.[1]
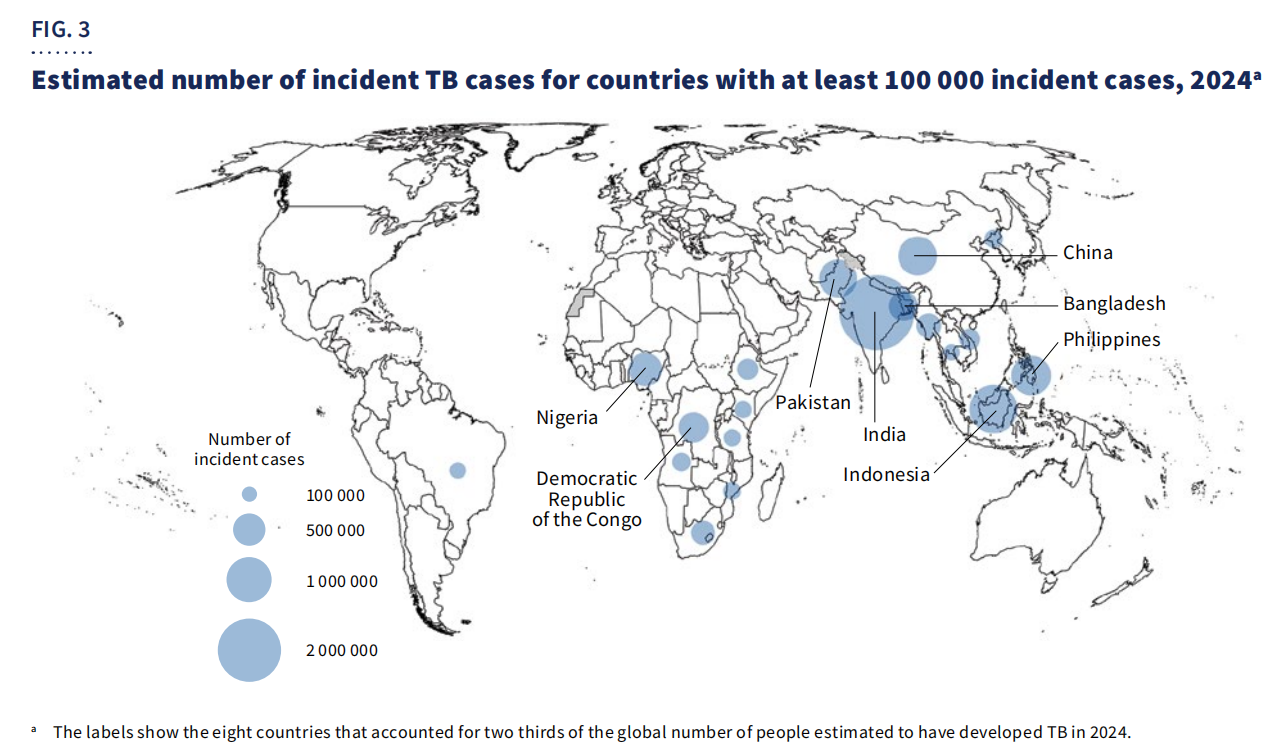
Geográficamente,67% de los casosSe concentraban en ocho países: India, Indonesia, Filipinas, China, Pakistán, Nigeria, la República Democrática del Congo y Bangladesh.
A pesar de los avances, la tuberculosis sigue siendo una de las principales causas de muerte entre las personas que viven con el VIH y un importante factor que contribuye a la mortalidad asociada a la resistencia a los antimicrobianos. La financiación mundial sigue siendo insuficiente, con solo5.900 millones de dólaresdisponible en 2024, muy por debajo de laObjetivo anual de 22 mil millones de dólaresprevisto para 2027.
Estas cifras ponen de relieve la urgente necesidad de fortalecer los programas de control de la tuberculosis a nivel mundial, centrándose en ampliar el acceso a los diagnósticos, mejorar los resultados del tratamiento y abordar los determinantes sociales que impulsan la transmisión de la tuberculosis. La tuberculosis sigue requiriendo una sólida cooperación internacional y un compromiso político para alcanzar los objetivos de la Estrategia para Acabar con la Tuberculosis.
Mycobacterium tuberculosis: Patogénesis y clasificación
Mycobacterium tuberculosis (MTB/M. tuberculosis) es el principal y más común patógeno responsable de la tuberculosis (TB). Puede ingresar al cuerpo humano a través de las vías respiratorias, el tracto digestivo o la piel y las membranas mucosas dañadas, infectando múltiples órganos y causando diferentes formas de TB. La TB pulmonar, que se transmite principalmente por gotitas, representa más del 80 % de los casos de TB. Los síntomas comunes incluyen tos, producción de esputo y hemoptisis. Después de la infección en los pulmones, la bacteria puede propagarse a través del torrente sanguíneo a múltiples sistemas, lo que puede provocar TB esquelética, urinaria o gastrointestinal.[2]
MTB forma parte del género Mycobacterium, que incluye:
- Complejo de Mycobacterium tuberculosis (MTBC): Compuesto por M. tuberculosis, M. bovis, M. africanum, M. canettii y M. microti, entre otros. Si bien M. tuberculosis es la causa principal de la tuberculosis, M. bovis y M. africanum también pueden inducir la enfermedad.
- Micobacterias no tuberculosas (MNT).
- Mycobacterium leprae, la causa de la lepra.
Métodos de diagnóstico de laboratorio
Un diagnóstico preciso y oportuno es esencial para un control eficaz de la tuberculosis. La Organización Mundial de la Salud subraya queLas tecnologías de diagnóstico molecular rápido han transformado fundamentalmente la detección de la tuberculosis al permitir la identificación altamente sensible y específica de patógenos, al tiempo que detectan la resistencia a los medicamentos.[1].
- Microscopía y cultivoe: El cultivo sigue siendo el método de referencia para el diagnóstico de la tuberculosis, ya que permite la identificación definitiva de microorganismos viables y facilita las pruebas de sensibilidad a los fármacos y el análisis genómico. Sin embargo, debido a la lenta tasa de crecimiento de Mycobacterium tuberculosis, los resultados suelen tardar entre 2 y 8 semanas, lo que limita su utilidad clínica en la toma de decisiones urgentes.
-Pruebas inmunológicas: Los métodos inmunológicos, como la prueba cutánea de tuberculina (PPD) y las pruebas de liberación de interferón gamma (IGRA), detectan las respuestas inmunitarias del huésped a la infección por tuberculosis. Si bien son útiles para identificar la infección latente, estas pruebas no permiten distinguir de forma fiable entre la infección activa y la previa, por lo que su especificidad diagnóstica es limitada en entornos con alta prevalencia de la enfermedad.
-Diagnóstico molecular (NAAT): Se recomiendan las pruebas basadas en ADN, como la amplificación de ácidos nucleicos (NAAT), por su alta sensibilidad y especificidad.
-Secuenciación dirigida de próxima generación (tNGS): Las tecnologías de secuenciación dirigida proporcionan una identificación de alta resolución de las mutaciones asociadas a la resistencia. Las directrices de la OMS recomiendan la tNGS como una herramienta avanzada para la detección de la resistencia a los fármacos después del diagnóstico, lo que respalda las estrategias de tratamiento de precisión [3].
-Secuenciación metagenómica de próxima generación (mNGS): La secuenciación metagenómica permite la detección imparcial de una amplia gama de patógenos sin necesidad de selección previa del objetivo. Este enfoque resulta especialmente valioso en situaciones clínicas complejas o poco claras, como infecciones mixtas y pacientes inmunocomprometidos, donde los métodos de diagnóstico convencionales pueden ser insuficientes.
La OMS destaca además que la confirmación microbiológica es esencial para iniciar la terapia adecuada y mejorar los resultados de los pacientes, reforzando la importancia de integrar diagnósticos moleculares avanzados en los programas de control de la tuberculosis [1].
Soluciones integrales de diagnóstico molecular de Macro & Micro-Test.
1.Detección de tuberculosis y resistencia a los medicamentos mediante PCR múltipletuberculosis
| Código de producto | Nombre del producto | Proceso de dar un título |
| HWTS-RT001 | Kit de detección de ADN de Mycobacterium tuberculosis (PCR de fluorescencia) | CE |
| HWTS-RT137 | Kit de detección de mutaciones de resistencia a la isoniazida en Mycobacterium tuberculosis (curva de fusión) | CE |
| HWTS-RT074 | Kit de detección de ácido nucleico de Mycobacterium tuberculosis y resistencia a la rifampicina (curva de fusión) | CE |
| HWTS-RT102 | Kit de detección de ácidos nucleicos basado en amplificación isotérmica con sonda enzimática (EPIA) para Mycobacterium tuberculosis | CE |
| HWTS-RT144 | Kit de detección de ácidos nucleicos del complejo Mycobacterium tuberculosis liofilizado (amplificación isotérmica con sonda enzimática) | CE |
| HWTS-RT105 | Kit de detección de ADN de Mycobacterium tuberculosis liofilizado (PCR por fluorescencia) | CE |
| HWTS-RT147 | Kit de detección de ácido nucleico de Mycobacterium tuberculosis y resistencia a rifampicina e isoniazida (curva de fusión) | CE |
Cuando existe una fuerte sospecha clínica de tuberculosis (TB),HWTS-RT147Se recomienda esta prueba para la detección cualitativa de la infección por MTB y la tuberculosis multirresistente (TB-MDR). Esta prueba identifica mutaciones en el gen.gen rpoB, que conducen a la resistencia a la rifampicina (RIF) y mutaciones en el genGenes katG e InhA, que están asociadas con la resistencia a la isoniazida (INH). Proporciona una prueba eficaz y única para MTB y TB-MDR, incorporando un control de calidad interno para minimizar los resultados falsos negativos, lo que garantiza resultados rápidos y precisos.
2.Secuenciación dirigida PTNseq para la detección de patógenos respiratorios y la elaboración de perfiles de resistencia.
| Código de producto | Nombre del producto | Especulación. |
| HWKF-TS0001 | Kit de enriquecimiento de genes de patógenos de infecciones del torrente sanguíneo PTNseq | 24 pruebas/kit |
| HWKF-TS0002 | Kit de enriquecimiento genético de microorganismos patógenos para infecciones del sistema nervioso central PTNseq | 24 pruebas/kit |
| HWKF-TS0003 | Kit de enriquecimiento de genes de patógenos de infecciones respiratorias PTNseq | 24 pruebas/kit |
| HWKF-AT0003 | Kit de construcción de bibliotecas de enriquecimiento automatizado (ONT) para microorganismos patógenos de infecciones respiratorias PTNseq | 24 pruebas/kit |
| HWKF-TS0004 | Kit de enriquecimiento genético de patógenos infecciosos de amplio espectro PTNseq | 24 pruebas/kit |
| HWKF-TS0005 | Kit de enriquecimiento genético de microorganismos patógenos infecciosos de espectro ultra amplio PTNseq | 24 pruebas/kit |
| HWKF-TS0151 | Kit de tipificación de micobacterias y enriquecimiento de genes de resistencia a fármacos (método de amplificación múltiple) | 24 pruebas/kit |
En casos de infecciones respiratorias mixtas (incluidas infecciones de las vías respiratorias superiores e inferiores, tuberculosis y enfermedades respiratorias crónicas), o cuando se requiere un análisis de genes de resistencia a los medicamentos (por ejemplo, sospecha de tuberculosis resistente a los medicamentos),Serie PTNseq de detección de genes dirigida de alto rendimientoSe puede aplicar. Basado en tecnología avanzada de secuenciación dirigida, PTNseq emplea PCR ultra-multiplex para enriquecer secuencias objetivo específicas, combinada con secuenciación de alto rendimiento y tecnología de nanoporos de tercera generación para la identificación integral de patógenos y la elaboración de perfiles de resistencia a los medicamentos.
El sistema utiliza cebadores patentados de alta especificidad para la amplificación ultra-multiplex de genes objetivo. Respaldado por una base de datos propia y algoritmos bioinformáticos inteligentes, proporciona una identificación precisa de patógenos junto con el análisis de genes de resistencia a fármacos y virulencia. El enriquecimiento dirigido reduce la interferencia del ADN del huésped, mejorando la sensibilidad en muestras con un alto fondo humano y permitiendo la detección eficaz de objetivos difíciles comoMycobacterium tuberculosishongos, bacterias intracelulares, virus de ARN y genes de resistencia o virulencia.
PTNseq alcanza un límite de deteccióntan bajo como 100 copias/mly cubre175 patógenos respiratorios comunes, incluidos 76 bacterias, 73 virus, 19 hongos, 7 micoplasmas, así comoClamidia, Rickettsiay 54 genes de resistencia a los medicamentosEl panel incluye elMycobacterium tuberculosisMicobacterias no tuberculosas complejas e importantes.
La serie PTNseq combina alta sensibilidad con rentabilidad, mejorando las tasas de detección de patógenos y facilitando la terapia antimicrobiana individualizada, a la vez que ayuda a mitigar la resistencia a los antimicrobianos. Integrada con el sistema automatizado de preparación de bibliotecas para secuenciación genética (AIOS), ofrece una solución hospitalaria optimizada con un tiempo de respuesta de tan solo 6,5 horas desde la toma de la muestra hasta el resultado.

3. Secuenciación metagenómica para la detección de patógenos de amplio espectro.
| Código de producto | Nombre del producto | Especulación. |
| HWKF-MN0011 | Kit de detección de patógenos metagenómicos (ADN-Illumina) | 24 pruebas/kit |
| HWKF-MN0018 | Kit de detección de patógenos metagenómicos (ADN-MGI) | 24 pruebas/kit |
| HWKF-MN0021 | Kit de detección de patógenos metagenómicos (DNA-ONT) | 24 pruebas/kit |
| HWKF-MN0012 | Kit de detección de patógenos metagenómicos (ARN-Illumina) | 24 pruebas/kit |
| HWKF-MN0019 | Kit de detección de patógenos metagenómicos (ARN-MGI) | 24 pruebas/kit |
| HWKF-MN0022 | Kit de detección de patógenos metagenómicos (RNA-ONT) | 24 pruebas/kit |
| HWKF-MN0013 | Kit de detección de patógenos metagenómicos (ADN+ARN-Illumina) | 24 pruebas/kit |
| HWKF-AYM0013 | Kit de construcción de bibliotecas automatizadas para la detección de patógenos metagenómicos (ADN+ARN-Illumina) | 24 pruebas/kit |
| HWKF-MN0020 | Kit de detección de patógenos metagenómicos (ADN+ARN-MGI) | 24 pruebas/kit |
| HWKF-MN0023 | Kit de detección de patógenos metagenómicos (ADN+ARN-ONT) | 24 pruebas/kit |
Cuando el diagnóstico clínico no está claro,Detección genética de alto rendimiento de patógenos mediante mNGSSe puede realizar en varias muestras del paciente, incluyendo líquido de lavado broncoalveolar, esputo, hisopos faríngeos, sangre, derrame pleural, pus y muestras de tejido. Este enfoque utiliza tecnología de secuenciación metagenómica, donde diferentes muestras se someten a un pretratamiento dirigido seguido de la extracción de ácidos nucleicos utilizando perlas de vidrio y enzimas digestivas de la pared celular, lo que mejora la eficiencia de la extracción. La secuenciación se adapta a múltiples plataformas, lo que garantiza un alto volumen de datos para mejorar la sensibilidad de mNGS y la integridad del ensamblaje. Los datos se analizan utilizando una base de datos propia y algoritmos inteligentes para detectarmás de 20.000 patógenos, incluyendo bacterias, hongos, virus y parásitos, proporcionando información sobre microorganismos patógenos sospechosos. Este método es adecuado para pacientes difíciles de diagnosticar, gravemente enfermos o inmunocomprometidos, incluyendo la identificación deMTBcomplejoyNTM, así como infecciones mixtas. Mejora significativamente las tasas de detección de patógenos y ayuda a orientar el uso clínico específico de antibióticos, lo que permite un diagnóstico preciso de la infección.
Conclusión
Aunque se han logrado avances sustanciales, la tuberculosis sigue siendo un importante desafío para la salud mundial, en particular en el contexto de la resistencia a los medicamentos, la falta de financiación y el acceso desigual a los diagnósticos.
La OMS subraya que ampliar el acceso a diagnósticos moleculares rápidos y tecnologías de secuenciación avanzadas es fundamental para alcanzar los objetivos de la Estrategia para Acabar con la Tuberculosis. Con la innovación continua, la inversión y la colaboración mundial, erradicar la tuberculosis ya no es una aspiración, sino un objetivo alcanzable.
Referencias:
- Organización Mundial de la Salud. Informe mundial sobre la tuberculosis 2024/2025: Pruebas diagnósticas y tratamiento.
- Organización Mundial de la Salud. Manual de la OMS para la selección de pruebas de diagnóstico rápido moleculares recomendadas por la OMS para la detección de la tuberculosis y la tuberculosis resistente a los medicamentos.
- Organización Mundial de la Salud. Directrices consolidadas de la OMS sobre la tuberculosis: Módulo 3 – Diagnóstico (Actualización de 2024).
Fecha de publicación: 24 de marzo de 2026
