- 1. Carga mundial del cáncer de cuello uterino y desafíos de la detección precoz
El cáncer de cuello uterino sigue siendo un importante desafío para la salud pública mundial, a pesar de ser en gran medida prevenible mediante la detección temprana y la intervención eficaz. Según la Organización Mundial de la Salud (OMS), se estima que en 2022 se produjeron 662 000 nuevos casos y 349 000 muertes en todo el mundo, lo que lo sitúa como el cuarto cáncer más común y la cuarta causa principal de mortalidad relacionada con el cáncer entre las mujeres. La carga de la enfermedad se concentra de manera desproporcionada en los países de ingresos bajos y medianos (PIBM), donde las tasas de incidencia y mortalidad son significativamente más altas que en los países de ingresos altos. Esto se debe principalmente a la falta de programas de detección de alta calidad y a la detección y el tratamiento eficaces de las lesiones precancerosas, agravado por:
-Infraestructura de detección deficiente o inexistente: Falta de servicios de detección accesibles y con garantía de calidad.
-limitaciones de recursosInfraestructura de laboratorio limitada, logística de cadena de frío deficiente y suministro eléctrico poco fiable.
-escasez de mano de obra: Falta de personal de laboratorio y clínico capacitado.
-Retrasos y pérdida de seguimiento: Tiempo de demora entre la toma de muestras y la disponibilidad de los resultados, lo que conlleva retrasos en el manejo clínico o la pérdida de pacientes para el seguimiento[1].
2. Etiología y bases moleculares de la carcinogénesis cervical
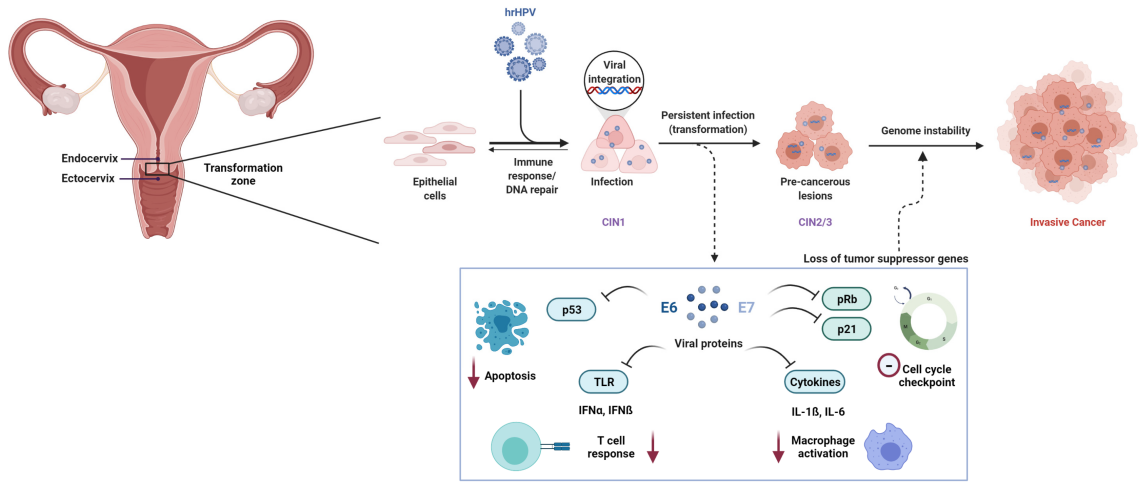
La infección persistente por el virus del papiloma humano de alto riesgo (VPH-AR) es una causa necesaria del cáncer de cuello uterino. Entre los más de 200 genotipos de VPH identificados, al menos12 tiposHan sido clasificados como cancerígenos (Grupo 1) por la Agencia Internacional para la Investigación del Cáncer (IARC).

A nivel molecular, la carcinogénesis mediada por el VPH está impulsada principalmente por las oncoproteínas virales E6 y E7. La E6 promueve la degradación de la proteína supresora de tumores p53, mientras que la E7 inactiva funcionalmente la proteína del retinoblastoma (Rb), lo que resulta en una desregulación del ciclo celular y una transformación maligna.
3.Estrategias de cribado recomendadas por la OMS
La Organización Mundial de la Salud recomienda la prueba de detección de ácidos nucleicos del VPH (NAT) como método de cribado primario preferido para la prevención del cáncer de cuello uterino.
Población general:Pruebas de amplificación de ácidos nucleicos (NAT) basadas en ADN o ARNm del VPH
Mujeres que viven con el VIH:Pruebas de amplificación de ácidos nucleicos (NAT) basadas en ADN del VPH
Intervalos de cribado:
Mujeres de entre 30 y 65 años: Cada 5-10 años
Mujeres que viven con el VIH: Cada 3-5 años
En comparación con los métodos basados en citología, las pruebas de VPH demuestranmayor sensibilidady proporcionaun valor predictivo negativo superior, lo que permite intervalos de detección más largos y rentables.
4.Perfil de producto objetivo de la OMS para las pruebas de detección del VPH
La OMS ha desarrollado unPerfil del producto objetivo (TPP)para ensayos de detección del VPH destinados a ser utilizados en entornos descentralizados y con recursos limitados.[1]
Las características clave incluyen:
- Compatibilidad con especímenes recolectados por el propio usuario.
- Detección de múltiples genotipos de VPH de alto riesgo (≥12 tipos)
- Operación por personal no capacitado en laboratorio
- Resultados disponibles en una sola consulta clínica.
Estos criterios respaldan las pruebas en el punto de atención y las estrategias de "detección y tratamiento".
5.Plataforma totalmente automatizada para la detección del VPH de alto riesgo.
El sistema AIO800 de Macro & Micro-Test proporcionaun flujo de trabajo totalmente automatizado desde la muestra hasta la respuestaIntegrar la extracción, amplificación y detección de ácidos nucleicos de acuerdo con las estrategias de cribado recomendadas por la OMS.

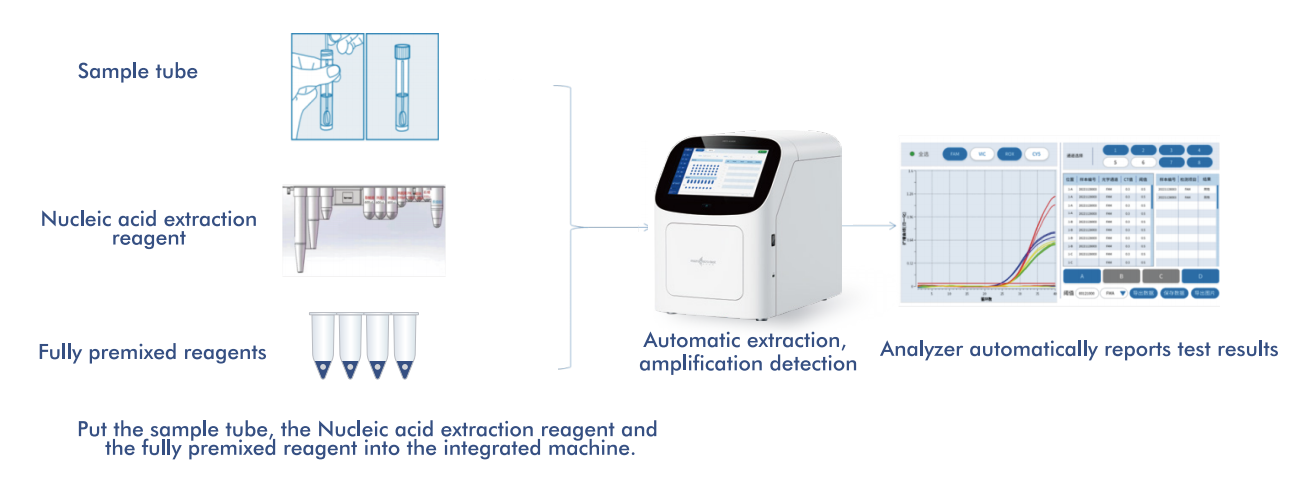
5.1 Flujo de trabajo automatizado de muestra a respuesta
La plataforma integra la extracción, amplificación y detección de ácidos nucleicos en un único sistema cerrado, que requiere una mínima intervención del operador. Este diseño:
- -Reduce la dependencia del personal de laboratorio especializado
- -Minimiza la variabilidad del proceso y el riesgo de contaminación.
- -Permite su implementación en entornos sanitarios descentralizados.
Al mismo tiempo, su capacidad de procesamiento permite su aplicación en laboratorios centralizados, facilitando así programas de cribado a gran escala.
5.2 Amplia cobertura de genotipado
El sistema detecta 14 tipos de VPH de alto riesgo, incluidos los 12 tipos cancerígenos clasificados por la IARC (VPH16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58 y 59), así como el VPH66 y el VPH68.
Es importante destacar que proporcionagenotipado específico de tiporesultados, lo que permite la estratificación del riesgo y una gestión clínica más precisa.
5.3 Sensibilidad analítica e implicaciones clínicas
Con un límite de detección de 300 copias/mL, el sistema es capaz de identificar infecciones por VPH de bajo nivel que contribuyen a:
- -Detección más temprana de infecciones clínicamente relevantes
- -Valor predictivo negativo mejorado
- -Apoyo a intervalos de cribado prolongados
5.4 Soporte para el automuestreo
La plataforma es compatible con ambosmuestras de hisopado cervical y muestras de orina autotomadasen consonancia con las recomendaciones de la OMS para abordar las principales barreras a la adopción de los programas de cribado, entre las que se incluyen:
- -Acceso limitado a centros de atención médica
- -Restricciones socioculturales
Fecha de publicación: 27 de marzo de 2026
